Химия и повседневная жизнь человека - поурочные разработки
Превращение соединений азота в почве и в растениях. Выращивание экологически чистых овощей - Сценарии прикладных уроков
С биологической точки зрения азот более ценен, чем любой из драгоценных металлов.
В. Л. Омеяянский
Цели урока. Организовать повторение свойств важнейших неорганических и органических соединений азота; ознакомить учащихся с превращениями этих соединений в почве и в растениях; научить применять знания, полученные из курса химии, для решения конкретных практических задач, связанных с производством сельскохозяйственной продукции.
Оборудование. Таблицы «Круговорот азота в природе», «Признаки азотного голодания у растений», «Допустимые нормы содержания нитратов в овощах», «Накопление нитратов в различных частях продуктивных органов растений» (приложение 5). Можно также подготовить для сравнения два комнатных растения (например, бальзамин) — с признаками азотного голодания и нормально обеспеченного азотом.
Ход урока
Начинают урок с краткого повторения основных вопросов: положение азота в периодической системе, строение атома, степени окисления, важнейшие соединения (аммиак, соли аммония, нитраты, аминокислоты, белки), нахождение в природе, условия связывания атмосферного азота. Отмечают, что азот — один из важнейших биогенных элементов.
После краткого повторения останавливаются более подробно на способах поглощения азота растениями. Из курса биологии учащиеся знают, что большинство растений, за исключением бобовых культур, поглощают азот только в виде ионов NH4+ и NO3-. Рассматривают пути и формы поступления азота в почву: минеральные удобрения представляют собой соединения, содержащие NH4+ и NO3-, а в органических удобрениях азот включен в белковые соединения. В такой форме азот не может усваиваться растениями и должен предварительно минерализоваться.
Минерализация — превращение органических соединений азота в неорганические. В общем виде этот процесс можно представить следующей схемой:
белки → аминокислоты → аммиак → нитриты → нитраты → молекулярный азот.
Если для облегчения понимания принять, что в органических соединениях азот находится только в составе аминогрупп — NH2, то схема его превращения будет выглядеть следующим образом:
![]()
Рассматривают подробно каждый этап минерализации.
Первая стадия распада органических азотсодержащих веществ до аммиака называется аммонификацией. Она протекает под действием почвенных микроорганизмов (аммонифицирующие бактерии), которые выделяют необходимые протеолитические ферменты. Таким образом, аммонификацию можно отнести к каталитическим процессам. Для объяснения химической сущности этого процесса необходимо написать уравнения реакций гидролиза белка (любого дипептида); превращения аминокислоты в аммиак (схематично); взаимодействия аммиака с угольной кислотой почвенного раствора:
![]()
Вторая стадия — нитрификация — окисление аммиака до NO3-, происходящее под действием нитрифицирующих бактерий:
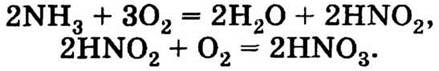
При этом важно отметить, что в почвенном растворе постоянно присутствуют катионы, которые образуют соли с нитрит- и нитрат-анионами.
Параллельно с аммонификацией и нитрификацией в почве протекает и процесс денитрификации — восстановления нитрат-ионов под действием денитрифицирующих бактерий до молекулярного азота по схеме:
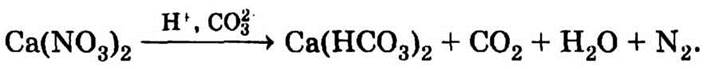
Таким образом, очевидно, что аммонификация и нитрификация способствуют накоплению в почве доступного для растений азота и повышению урожайности сельскохозяйственных культур; а денитрификация оказывает противоположное, негативное, действие.
А можно ли управлять процессом минерализации? С точки зрения биологии для аммонификации и нитрификации необходимы условия, обеспечивающие нормальную жизнедеятельность аммонифицирующих и нитрифицирующих микроорганизмов, т. e. достаточное количество влаги, воздуха, определенная температура. Исследования показали, что оптимальные условия для минерализации азота в почве — это влажность 60—70%, температура 25—32 °С, близкая к нейтральной реакция почвенного раствора, хорошая аэрация. Денитрификация интенсивно идет в анаэробных условиях, в переувлажненной почве с щелочной реакцией среды, в присутствии избытка доступного микроорганизмам органического вещества.
Исходя из этого, для усиления минерализации необходимо хорошо обрабатывать почву, обеспечивать ее аэрацию (не допускать образования почвенной корки), известковать кислые почвы, вносить достаточное количество органических удобрений (навоз, перегной). В то же время внесение в почву избытка древесных опилок, например с компостами, может привести к усилению денитрификации.
Кроме того, необходимо иметь в виду, что существуют азотфиксирующие бактерии, способные фиксировать азот воздуха и превращать его в доступную для растений форму. Эти бактерии живут в симбиозе с бобовыми культурами. Примерно 1/3 связанного бобовыми азота остается в послеукосных и корневых остатках и после их минерализации может использоваться культурами, следующими за ними в севообороте. При хорошем урожае клевер может накапливать 150—160 кг/га, люпин— 100—170 кг/га, люцерна— 25—300 кг/га азота. Свободноживущие бактерии-азотфиксаторы ассимилируют до 5—6 кг/га азота.
Предлагают учащимся вопросы для обсуждения:
1. Какие этапы минерализации азота являются окислительно-восстановительными процессами?
2. Почему с точки зрения биологии для аммонификации и нитрификации необходима хорошая аэрация почвы?
3. Какими способами земледелец может повлиять на процессы аммонификации и нитрификации?
4. В чем с точки зрения химии сущность распространенного агротехнического приема — мульчирования почвы торфом?
5. Будет ли достаточно эффективно протекать нитрификация, если внести большое количество аммонийного азота в бедную гумусом почву?
Задание. Перечисленные ниже факторы распределите на две группы:
а) способствующие образованию и накоплению в почве доступных форм азота;
б) препятствующие этим процессам.
Избыточная влажность, частое рыхление, повышенная кислотность, низкие температуры, известкование почв, нейтральная реакция почвы, внесение органических удобрений, образование почвенной корки, мульчирование.
Затем переходят к рассмотрению превращений азотсодержащих веществ в растениях.
Нитраты, поступившие в растения, восстанавливаются (при участии металлсодержащих ферментов) через нитриты до аммиака, из которого затем образуются аминокислоты и белки. Иными словами, в растениях протекает цепь превращений, обратных тем, которые происходят в почве. Содержание белков в продукции определяет ее пищевую ценность, значит, земледелец должен добиваться наиболее полного перехода минерального азота, поступившего в растения, в состав органических веществ.
Заметим, что при недостатке азота растение медленно растет, имеет мелкие, бледные, преждевременно желтеющие листья; при избытке азота бурно развивается вегетативная часть растений, а генеративная (наряду с клубнями и корнеплодами) оказывается в угнетенном состоянии. Избыточное поступление азота в почву особенно опасно потому, что приводит к его накоплению в растениях.
Для самих растений нитраты и нитриты безвредны, а вот для травоядных животных они очень опасны, так как, попадая в организм, взаимодействуют с гемоглобином крови, превращая его в метгемоглобин (железо гема окислено до Fe3+), который уже не может служить переносчиком кислорода. Именно поэтому один из признаков острого отравления нитратами — синюшность кожных покровов. Кроме того, нитраты могут взаимодействовать с аминами, всегда присутствующими в живом организме, с образованием нитрозоаминов, обладающих мутагенными свойствами:
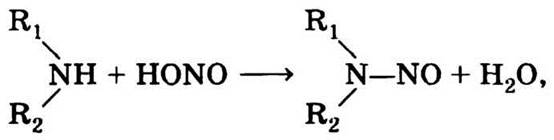
где R1, R2 — радикалы (алкиды).
Необходимо отметить, что нитраты и нитриты могут попадать в организм не только с овощами, но и с копченым мясом или рыбой.
Выясняют причины накопления нитратов в овощах.
В разные периоды вегетации ход процессов обмена азотистых веществ протекает по-разному. Наиболее интенсивно азот поглощается во время роста и развития стеблей и листьев. При созревании семян потребление азота из почвы практически прекращается. Белковые соединения, синтезированные в вегетативных частях растения, подвергаются гидролизу, продукты которого оттекают в репродуктивные органы, где вновь используются для синтеза белка. Нитраты, поступившие в этот период в растение, не превращаются в белки, а накапливаются в неизмененном виде.
В норме плоды, достигшие полной (биологической) зрелости, уже не содержат нитратов — произошло полное превращение соединений азота в белки. Но у многих овощей ценится именно незрелый плод (огурцы, кабачки). Вот почему они могут быть причиной отравления нитратами. Удобрять такие культуры азотными удобрениями желательно не позднее, чем за 2—3 недели до уборки урожая. Кроме того, полному превращению нитратов в белки препятствуют плохая освещенность, избыточная влажность и несбалансированность питательных элементов (недостаток фосфора и калия).
Как же избежать отравления нитратами и вырастить экологически чистую продукцию? Опасность отравления не следует преувеличивать, так как нитраты химически довольно активны и даже при обычном хранении к весне их содержание в плодах снижается на 30—50%. При мытье и чистке теряется 10—15%, при варке— 40—70%. Уменьшить вредное влияние нитратов на организм можно с помощью аскорбиновой кислоты: если ее соотношение с нитратами составляет 2:1, то нитрозоамины не образуются. Не следует увлекаться внесезонными тепличными овощами, например 2 кг тепличных огурцов, съеденных за один прием, могут вызвать опасное для жизни отравление нитратами.
Известны простые и эффективные приемы снижения уровня нитратов в овощной продукции, которые доступны каждому.
Например, перед употреблением тепличных зеленных овощей их надо поставить как букет в воду на подоконнике при ярком солнечном свете или под электрическую лампу на 1—2 часа. В листьях этих растений содержатся ферменты нитратредуктаза и нитритредуктаза, которые активируются светом и быстро восстанавливают нитрат-ионы до аминокислот и белков.
На свойствах нитрат- и нитритредуктазы основано действие и эффективного агротехнического
приема снижения уровня нитратов в растениях — обработка семян или посевов микроэлементами. Эти ферменты относятся к металлоферментам, в состав нитратредуктазы входит молибден, а нитритредуктазы — железо. При недостатке молибдена в почве активность нитратредуктазы снижается, что приводит к накоплению нитратов. Такой простой агротехнический прием, как замачивание семян овощей в течение суток в растворе (NH4)2MoО4 концентрации 0,01—0,05%, приводит к значительному снижению содержания нитратов в выращенной из этих семян продукции. Эффективно и опрыскивание вегетативной части овощей (моркови, свеклы) в период интенсивного формирования корнеплодов 0,01—0,1%-ным раствором (NH4)2MoО4.
Надо также знать, преимущественно в каких частях растения накапливаются нитраты и какими способами их можно удалить из различных овощей (приложение 5).
Оказывается, что показатели концентрации нитратов различаются и по сортам: в ранних они больше, чем в поздних.
В разных странах приняты разные ПДК содержания нитратов в продукции растениеводства. Всемирная организация здравоохранения (ВОЗ) считает допустимым содержание нитратов в диетических продуктах до 300 мг на 1 кг сырого вещества.
Знакомят учащихся с таблицей 5, которая отражает способность различных культур накапливать нитраты.
Для того чтобы оценить, насколько реальна опасность отравления нитратами, предлагают учащимся расчетные задачи.
1. В столовой свекле содержится в среднем 1200 мг нитрат-ионов на 1 кг. При очистке свеклы теряется 10% нитратов, а при варке — еще 40%.
Таблица 5. ПДК нитратов в продукции растениеводства, мг NO3- на 1 кг
|
Томаты |
60 |
|
Картофель |
80 |
|
Морковь |
300 |
|
Свекла столовая |
1400 |
|
Лук (перо) |
400 |
|
Огурцы (тепличные) |
150 |
|
Капуста |
300 |
|
Арбуз |
45 |
|
Дыня |
45 |
Будет ли превышена суточная норма потребления нитратов (325 мг), если ежедневно съедать по 200 г вареной свеклы?
2. Содержание нитратов в питьевой воде может достигать 45 мг/л (допустимая норма). Сколько воды надо выпить, чтобы потребление нитратов достигло максимально допустимой суточной дозы — 325 мг?
Переходят к рассмотрению вопроса о способах выращивания экологически чистой продукции растениеводства.
Прежде всего растениевод должен грамотно вносить азотные удобрения: в строго рассчитанных дозах и в оптимальные сроки. Выращивать овощи, особенно зеленные культуры, надо при хорошей освещенности, оптимальных показателях влажности почвы и температуры.
Необходимо отметить, что накопление нитратов в овощах возможно и при использовании только органических удобрений. Несвоевременное внесение навоза, особенно в избыточных дозах, приводит к тому, что поступившие в растение минеральные соединения азота не успевают полностью превратиться в белковые. В связи с этим можно обсудить диалог, услышанный на рынке.
Покупатель: Скажите, ваша петрушка не загрязнена нитратами?
Продавец: Что вы, их там не может быть, ведь мы удобряем почву только навозом.
А что же в будущем? Одним из перспективных направлений исследований ученых по проблеме обеспечения растений азотом является биотехнология связывания азота, основанная на пересадке генов, ответственных за фиксацию азота, другим бактериям или высшим растениям.
В заключение, чтобы закрепить знания, полученные на уроке, учащимся предлагают задания для самостоятельной работы.
1. Подумайте, в каких почвах будут активнее идти процессы минерализации азота — в глинистых или песчаных.
2. В свежем навозе значительное количество азота содержится в виде мочевины. Напишите схему превращения мочевины в нитраты и определите степень окисления азота на каждой ступени превращения.
3. Для каждого из указанных понятий подберите определение.
Понятия:
1) аммонификация;
2) минерализация;
3) нитрификация;
4) денитрификация.
Определения:
а) превращение органических соединений азота в неорганические;
б) окисление аммонийного азота до NО3-;
в) распад органических азотсодержащих соединений до аммиака;
г) восстановление NО3- до N2.
4. Распределите перечисленные требования по степени важности в борьбе с загрязнением сельхозпродукции нитратами.
Хорошая освещенность, соблюдение режима полива, соблюдение сроков внесения удобрений, соблюдение норм внесения удобрений.
5. Среди перечисленных ниже факторов отметьте те, которые влияют на накопление нитратов и сельхозпродукции.
Сорт, вид, сезон выращивания, освещенность, « роки уборки.
6. Зная причины и закономерности накопления нитратов в растениеводческой продукции, а также особенности употребления в пищу различных культур, попробуйте объяснить, почему именно тленные культуры являются чаще всего источником отравления нитратами.
Литература
1. Соколов О. Нитраты — под строгий контроль // Наука и жизнь. 1988. № 8. С. 69.
2. Лихолат Т. В. Снижение нитратов в продукции растениеводства // Школа и производство. 1997. №2. С. 71.
3. Скурихин И. М., Нечаев А. П. Все о пище с точки зрения химика. М.: Высшая школа, 1991.
4. Смирнов 77. М., Муравин Э. А. Агрохимия. М.: Агропромиздат, 1991.
5. Михалева М. В., Мартыненко Б. Б., Изилянова Э. М. Экспресс-анализ овощей на содержание нитратов // Химия в школе. № 1. 2003. С. 57.
1 Урок проводят в 11 классе.