Химия и повседневная жизнь человека - поурочные разработки
Война в огороде - Сценарии уроков на основе проблемных заданий
Цели урока. Дать учащимся знания прикладного характера, связанные с применением химических средств защиты растений.
Оборудование. В качестве наглядных средств на этом уроке можно использовать образцы пестицидов, поступающих в продажу, причем обязательно в фабричной упаковке, с инструкцией по применению, цветные таблицы с изображением признаков болезней сельскохозяйственных культур и их вредителей.
Методические рекомендации по проведению урока
В задания включена информация преимущественно о тех пестицидах, состав и свойства которых можно объяснить на основе программного материала по химии, о малотоксичных препаратах, которые могут быть использованы учащимися самостоятельно.
Можно провести демонстрационные опыты: определение кислотности раствора бордоской жидкости с помощью гвоздя или индикатора, взаимодействие бордоской и бургундской жидкостей с мылом, быстрое взаимодействие металлических предметов с сернистым газом.
Большинство заданий можно выполнить после изучения курса неорганической химии, т. е. в 9 классе, исключив задания, которые требуют знаний по органической химии, поэтому полностью урок можно проводить только в 11 классе.
Примерный текст введения к уроку
Каждый из вас, кто хоть когда-нибудь выращивал овощи или ягоды на даче, знает, что садоводу и огороднику приходится вести постоянную войну с вредителями и болезнями сельскохозяйственных культур. Как выиграть эту войну и не повредить своему здоровью?
Население нашей планеты все больше интересуется экологическими проблемами, качеством продуктов питания, воды и воздуха. Нарастает страх перед применением минеральных удобрений и пестицидов, все большим спросом пользуются экологически чистые сельхозпродукты (иногда их называют «органические овощи»), выращенные без удобрений и ядохимикатов. Но так ли велика опасность пестицидов? И можно ли выиграть войну в огороде без химического оружия? А если все же приходится его применять, то как не обратить это оружие против собственного здоровья?
Человек, знакомый с химией, получает в такой войне большое преимущество. Какие средства борьбы наименее опасны для человека? Как правильно рассчитать концентрацию рабочего раствора и приготовить его? Чем заменить отсутствующий препарат? Эти вопросы неизбежно рано или поздно возникают у каждого огородника. Цель нашего урока — научить вас самостоятельно находить ответы на них.
Задания
11.1. Препараты для борьбы с грибными болезнями растений называют фунгицидами (от лат. fungus — гриб и caedo — убиваю). Один из самых распространенных фунгицидных препаратов — бордоская жидкость, которую готовят смешиванием водного раствора медного купороса и суспензии свежегашеной извести. В результате образуется водная суспензия, содержащая Cu(OH)2, CuSО4, CaSО4 в молярном соотношении 3:1:1, а также основный сульфат меди (II). Для образования стойкой суспензии весовое соотношение CuSO4 · 5Н2O : Са(ОН)2должно составлять 1:0,75. Но если известь не свежегашеная, ее следует брать в избытке. Почему?
11.2. При обработке деревьев бордоской жидкостью норма расхода 10—20 кг/га медного купороса, а при обработке суспензией хлорокиси меди (II), формула которой 3Сu(ОН)2 · СuСl2 · Н2O, — 3,6—7,2 кг/га всего препарата. Какой из двух препаратов предпочтительнее с точки зрения экологии?
11.3. Бордоская жидкость— водная суспензия, примерный состав которой:
![]()
Хорошая бордоская жидкость должна иметь нейтральную или слабощелочную реакцию, так как кислотные растворы повреждают листья, а сильнощелочные плохо удерживаются на поверхности. На практике, чтобы проверить кислотность приготовленного состава, в него опускают гвоздь. Если реакция раствора кислотная, на поверхности гвоздя появляется налет меди, тогда в препарат добавляют известкового молока. В результате какой химической реакции образуется налет меди на гвозде и почему этого не происходит в щелочной среде? И можно ли обойтись без гвоздя?
11.4. Фунгицидный препарат — бургундскую жидкость готовят смешиванием раствора медного купороса с раствором кальцинированной соды. Для получения устойчивой суспензии основного карбоната меди состава 3Сu(ОН)2 · 2СuСO3 на 1 кг медного купороса берут 0,5 кг кальцинированной соды (безводного Na2CO3). Если у вас нет безводного Na2CO3, а есть только кристаллическая сода Na2CO3 · 10Н2O, сколько ее надо взять для получения суспензии такого же состава?
11.5. Почему при расчете нормы расхода бордоской и бургундской жидкостей за основу берут количество медного купороса? Попробуйте также объяснить происхождение названий этих фунгицидных препаратов.
Подсказка. В учебнике географии.
11.6. Для лучшего прилипания фунгицидных препаратов к листьям растений в рабочие растворы можно добавлять силикатный клей, молоко, казеиновый клей, мыло. Почему в бургундскую жидкость, которую готовят из медного купороса и кальцинированной соды, можно добавлять любые из перечисленных веществ, а в бордоскую жидкость, которую приготавливают из медного купороса и суспензии гашеной извести, нельзя добавлять мыло?
11.7. Можно ли готовить бордоскую и бургундскую жидкости в баках из алюминия или оцинкованной жести?
11.8. Для борьбы с почковым клещом черной смородины очень эффективен известково-серный отвар (ИСО). Действующее вещество ИСО — полисульфиды кальция, которые образуются в очень жестких условиях: при кипячении в течение двух часов смеси воды, серы и гашеной извести в весовом соотношении 17:2:1. Кипятить смесь надо на открытом воздухе, на костре, что очень неудобно. Можно приготовить и «самосваривающийся» ИСО из 3,6 кг негашеной извести, 2,4 кг серы и 100 л воды. Взаимодействие протекает медленно, несколько часов, но зато позволяет избежать неудобств, связанных с кипячением на костре. Какой химический процесс позволяет приготовить ИСО без помощи костра?
11.9. Малотоксичный препарат для борьбы с вредителями и болезнями сельскохозяйственных культур можно приготовить из древесной золы: одну литровую банку золы надо прокипятить в 4 л воды в течение часа, охладить, профильтровать, добавить 10—20 г мыла. Что является основным действующим началом в этом препарате и к какой группе пестицидов его можно отнести — органических или неорганических?
Подсказка. Термином «пестициды» обозначают всю совокупность химических средств защиты растений от болезней и вредителей.
11.10. Как вы думаете, представляет ли какую-то ценность для огородника остаток после выщелачивания (так называют описанный в задании 11.9 процесс извлечения из золы водорастворимых веществ) золы или его можно без сожаления выбрасывать?
11.11. Доступный и малотоксичный препарат для борьбы с мучнистой росой крыжовника — 0,5%-ный водный раствор кальцинированной соды, в который для прилипаемости добавляют мыло. Если нет кальцинированной соды, раствор можно приготовить и из кристаллической соды Na2CO3 · 10Н2O или питьевой соды NaHC03. Сколько надо взять кристаллической соды или питьевой соды, чтобы приготовить 10 л раствора, равноценного по активности 0,5%-ному раствору Na2CO3? Принять для расчетов, что плотность полученных растворов равна 1.
11.12. Фунгицидными и бактерицидными свойствами обладают водные растворы хорошо известных солей натрия: Na2CO3 и Na2HPO4. Действующим веществом этих пестицидов являются ионы натрия, присутствующие в их водных растворах. Какую соль — Na2CO3, Na2CO3 · 10Н2O или Na2HPO4 — целесообразнее использовать для этих целей, если их стоимость примерно одинакова?
11.13. Для борьбы с мучнистой росой крыжовника можно использовать водные растворы (Na2CO3 или Na2HPO4), в которых действующим началом являются ионы натрия. Если используют кальцинированную соду, готовят раствор 0,5%-ной концентрации. Раствор какой концентрации надо приготовить из Na2HPO4, чтобы его активность соответствовала 0,5%-ному растворуNa2CO3?
11.14. Метальдегид, или металь, применяют для борьбы со слизнями. Он представляет собой полимер ацетальдегида формулы (СН3СНO)4. Препарат выпускают в виде приманки — гранул из отрубей, содержащих 5% метальдегида. Гранулы рассыпают на грядках, норма — 1,5 кг действующего вещества на гектар. Сколько препарата надо приобрести для однократной обработки огорода площадью 2 сотки?
11.15. Обычно слизни досаждают тем огородникам, у которых грядки расположены в тени плодовых деревьев. Если вы рассыпали приманку с метальдегидом на грядки, можно ли обрабатывать яблони над этими грядками бордоской жидкостью?
11.16. Для обработки семенных клубней картофеля против грибных болезней применяют формальдегид СН2O. Рабочий раствор готовят разведением 40%-ного раствора формальдегида в соотношении 1 : 80, расход рабочего раствора 30 л на 1 т картофеля. Сколько вам потребуется формальдегида для обработки двух мешков (примерно 100 кг) посевного материала картофеля? Назовите это соединение в соответствии с современной номенклатурой.
11.17. Бутиламин С4Н9—NH2— фунгицид, особенно активный против плесневых грибов. Обычно его применяют для защиты плодов от гнили и плесени при транспортировке. Зная, что бутиламин — жидкость с температурой кипения 63 °С, взаимодействует с кислотами, образуя водорастворимые соли, также обладающие фунгицидным действием, предложите наиболее технологичный способ обработки плодов томатов. Как можно обезопасить себя от попадания остатков бутиламина в организм при потреблении плодов, прошедших такую обработку?
11.18. Нитрафен — пестицид широкого спектра действия — получают нитрованием каменноугольных фенолов. В продажу он поступает в виде 60% - ной пасты, из которой готовят 2%-ный рабочий раствор. Можете ли вы написать химическую формулу нитрафена?
11.19. Для обработки складских помещений, а также зерна, овощей и фруктов в складах и трюмах раньше применяли фумигацию парами некоторых хлорорганических и броморганических соединений, например дихлорэтана Cl—СН2СН2—Сl и бромистого метила СН3Вr. При этом дихлорэтан обычно использовали для обработки пустых складов, а бромистым метилом пользовались намного чаще — им обрабатывали как свежие, так и сухие фрукты, пищевое зерно, хотя чисто технологически дихлорэтан удобнее: это жидкость с температурой кипения 83,5 °С, а бромистый метил при температуре выше 4,6 °С — газообразное вещество, которое надо подавать из баллонов. Объясните, в чем заключается преимущество бромистого метила.
Помните, что многие галогенопроизводные углеводородов очень опасны для человека.
11.20. Вам надо провести обработку стеклянной теплицы на металлическом каркасе после сбора урожая и погреба перед закладкой продукции. У вас есть выбор между окуриванием серными шашками и обработкой дихлорэтаном. Какой способ вы предпочтете для каждого объекта?
11.21. Вы решили обработать дихлорэтаном пустой склад для овощей площадью 100 м3 и высотой 2,5 м. Сколько потребуется препарата при норме 300 г/м3 и где надо расположить мешковины, пропитанные дихлорэтаном, — на полу или в верхней части помещения?
11.22. Для обеззараживания складов, погребов, теплиц и парников можно применять окуривание сернистым газом — оксидом серы (IV). В обрабатываемом помещении поджигают серу и выдерживают его закрытым в течение 1—2 суток. Какое количество серы надо сжечь для обработки погреба размером 2 x 3 х 2 м, если рекомендуемая концентрация этого фумиганта 1:30 (1 объем SO2 на 30 объемов воздуха)?
11.23. При сжигании серы образуется оксид серы (IV) в результате реакции соединения. Но можно получить его для обработки погреба и путем реакции обмена. Какие для этого потребуются исходные вещества и как это лучше осуществить технологически?
Ответы и решения
11.1. При хранении гашеной извести происходит превращение Са(ОН)2 в СаСO3 за счет взаимодействия с СO2 воздуха, в результате общее количество Са(ОН)2 в извести уменьшается.
11.2. Прежде всего выясним, по какому параметру можно сравнить эффективность этих препаратов. Нормы обработки определяют агрохимики на основании специально проводимых опытов, поэтому эффективность препаратов целесообразно сравнить по количеству меди, которое попадет на 1 га плантаций при обработке этими препаратами.
M(CuSO4 · 5Н2O) = 250 г/моль.
В 250 г CuSO4 · 5Н2O — 64 г Сu,
в 10 кг CuSO4 · 5Н2O — х г Сu.
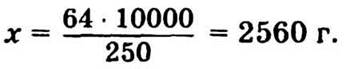
Таким образом, при обработке бордоской жидкостью при норме 10—20 кг медного купороса на 1 га попадет от 2560 до 5120 г меди.
М(3Сu(ОН)2 · СuСl2 · Н2O) = 447 г/моль.
В 447 г 3Сu(ОН)2 · СuСl2 · Н2O — 256 г Сu,
в 3,6 кг 3Сu(ОН)2 · СuСl2 · Н2O — х г Сu.
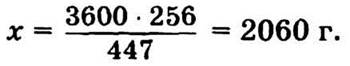
При обработке хлорокисью меди на 1 га попадет 2060 г меди. Хлорокись меди предпочтительнее, чем бордоская жидкость, с точки зрения экологии, так как при этом в окружающую среду попадает меньшее количество меди.
11.3. В бордоской жидкости медь находится преимущественно в виде суспензии основной соли Cu2(OH)2(SO4), которая плохо растворима в воде. Если реакция полученного препарата слабокислотная за счет гидролиза CuSO4, что имеет место при недостатке Са(ОН)2, основное количество меди находится в растворенном виде и может вытесняться из раствора железом в соответствии со своим положением в электрохимическом ряду напряжений:
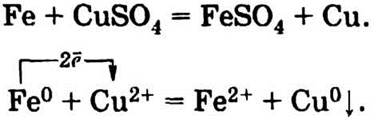
Химик может определить реакцию раствора и без гвоздя, с помощью индикаторной бумаги.
11.4. M(Na2CО3) = 106 г/моль,
М(Na2CО3 · 10Н2О) = 286 г/моль.
По условию задачи необходимо внести 500 г Na2CО3.
В 286 г Na2CО3 · 10Н2О — 106 г Na2CО3,
в х г Na2CО3 · 10Н2О — 500 г Na2CО3.
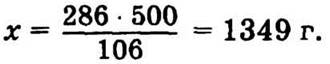
Таким образом, вместо 500 г Na2CО3 надо внести 1349 г Na2CО3 · 10Н2О.
Необходимо пересчитать и количество воды.
В 286 г Na2CО3 · 10Н2О — 180 г Н2О,
в 1349 г Na2CО3 · 10Н2О — х г Н2О.
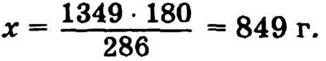
Общее количество воды для приготовления препарата надо уменьшить примерно на 850 г.
11.5. При расчете нормы расхода бордоской и бургундской жидкостей за основу берут количество медного купороса, потому что основное действующее вещество в этих препаратах — медный купорос. Название этих препаратов связано с географией Франции. Два региона этой страны — окрестности г. Бордо и Бургундия широко известны во всем мире как районы виноградарства и виноделия. Грибные болезни — настоящий бич виноградарей, и именно они предложили использовать для борьбы с этими болезнями составы, названные впоследствии бордоской и бургундской жидкостями.
11.6. Ионы кальция, содержащиеся в бордоской жидкости, образуют с мылом нерастворимые соединения (в основном стеарат кальция):
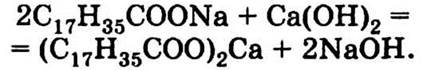
Этот осадок забивает отверстия опрыскивателя, что затрудняет обработку. В бургундской жидкости ионов кальция нет, поэтому для липкости к ней можно добавлять мыло.
11.7. См. ответы к уроку «Капитальный ремонт» — задания 8.12 и 8.19. Кроме того, если в процессе приготовления этих растворов их реакция окажется кислотной, возможно вытеснение меди из раствора цинком:
![]()
11.8. Реакция оксида кальция с водой протекает с выделением большого количества теплоты:
![]()
За счет выделяющегося тепла смесь настолько разогревается, что температура становится достаточной для образования полисульфидов кальция.
11.9. Зола состоит из неорганических соединений, главным образом карбонатов калия, магния, кальция. Основным действующим веществом является К2СО3, так что полученный препарат относится к неорганическим пестицидам.
11.10. При выщелачивании в раствор переходят прежде всего карбонаты калия, но в золе содержатся и другие соли — карбонаты и фосфаты кальция, магния, которые нужны растениям. Поэтому остаток после выщелачивания не следует выбрасывать. Его можно использовать как удобрение, хотя и медленно действующее, так как все легкорастворимые вещества перешли в раствор при выщелачивании.
11.11. Действующим веществом в этом растворе являются ионы натрия, которые образуются при диссоциации всех трех солей. При расчетах надо учитывать именно образующееся количество ионов натрия.
11.12. M(Na2CО3) = 106 г/моль, M(Na2CО3 · 10Н2О) = 286 г/моль. M(Na2HPО4) — 142 г/моль. Массовая доля натрия ω(Na+) в них составляет соответственно 43,6, 16 и 32,4%. Больше всего натрия содержится в кальцинированной соде Na2CО3, следовательно, именно ее и следует использовать для этих целей. Это позволит сэкономить средства на перевозке и хранении препаратов.
11.13. M(Na2CО3) = 106 г/моль, М(Na2HPО4) = 142 г/моль. Массовая доля натрия в этих солях составляет соответственно 43,4 и 32,4%. Если из Na2CО3 надо приготовить 0,5%-ный раствор, то из Na2HPО4:
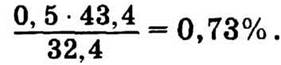
11.14. Находим, в каком количестве продажного препарата будет содержаться 1,5 кг метальдегида.
В 100 г препарата — 5 г ацетальдегида,
в х препарата — 1500 г ацетальдегида.
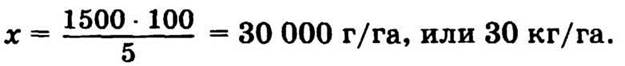
Находим массу порции для 0,02 га.
На 1 га — 30 кг,
на 0,02 га — х кг.
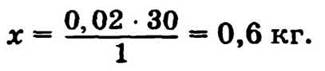
Обратите внимание: металь — сокращенное от метаацетальдегид, ацетальдегид иногда называют историческим названием — альдегид уксусной кислоты, в соответствии с современной номенклатурой это соединение называют также этаналь.
11.15. В бордоской жидкости содержится гидроксид меди (II), который взаимодействует с альдегидами, окисляя их до кислот, при этом медь со степенью окисления +2 восстанавливается до +1 и образуется Сu2O:
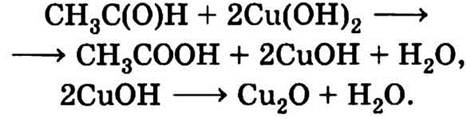
Эти реакции протекают при нагревании, но нельзя полностью исключить возможность их частичного протекания и при обычных температурах. Поэтому лучше не опрыскивать бордоской жидкостью деревья над грядками, где рассыпан метальдегид. Часть метальдегид а может превратиться в уксусную кислоту и потерять свою активность в отношении слизней.
11.16. На 1000 кг картофеля потребуется 30 л раствора,
на 100 кг — х.
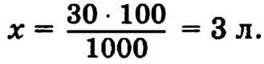
Если раствор получен разбавлением 1:80, то 3 л составляют 80 частей, 1 часть — х.
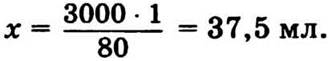
Для обработки двух мешков картофеля надо 37,5 мл 40%-ного раствора формальдегида. В аптеках под названием формалин продают 35—40%-ный раствор формальдегида с добавкой небольшого количества муравьиной кислоты НСООН. Для ваших целей достаточно приобрести один пузырек — 50 мл этого препарата.
Точное название формальдегида — метаналь, иногда используют также исторически сложившееся название «альдегид муравьиной кислоты». Муравьиную кислоту по современной номенклатуре следует называть метановой кислотой.
11.17. Самый простой способ обработки этим препаратом — фумигация, так как вещество будет легко испаряться. Фумигация (от лат. fumigatio — окуривание) — способ борьбы с сельскохозяйственными вредителями и возбудителями болезней растений, основанный на применении ядовитых паров, газа, дыма, аэрозолей, выделяемых специальными веществами — фумигантами. Емкость с бутиламином поместить в закрытую камеру с плодами или устроить укрытие типа палатки из полиэтиленовой пленки. Можно немного подогревать с помощью водяной бани для лучшего испарения. Пары бутиламина оседают на плодах и могут попасть в организм, поэтому перед употреблением их необходимо тщательно промыть водой, а для надежности — слабым раствором уксусной кислоты, так как амины обладают основными свойствами и лучше растворяются в кислой среде:
![]()
11.18. Точную формулу нитрафена написать нельзя, так как нитрафен не является чистым веществом, а представляет собой смесь нескольких веществ одной химической природы. Каменноугольные фенолы — смесь моно-, ди- и трифенолов, а также крезола, при их нитровании также образуется смесь продуктов, в молекулах которых содержится различное число нитрогрупп.
11.19. При выборе фумигантов учитывают легкость последующей дегазации: бромистый метил полностью улетучивается и не оседает на поверхности продуктов, а пары дихлорэтана могут конденсироваться на продуктах и попасть в организм человека. Поэтому его лучше использовать только для обработки пустых складов, трюмов.
11.20. В теплице поджигать серные шашки нельзя, так как SO2 вызовет сильную коррозию металлического каркаса:
![]()
Поэтому теплицу лучше обработать дихлорэтаном, а погреб окурить сернистым газом.
11.21. Объем помещения 100 · 2,5 = 250 м3, расход препарата составит 300 · 250 = 75 000 г, мешковину надо расположить под потолком, так как дихлорэтан намного тяжелее воздуха.
11.22. Объем погреба 12 м3, или 12 000 см3, или 12 000 л. Для эффективной обработки надо получить 12 000 : 30 = 400 л газа.
Оксид серы (IV) образуется по реакции, уравнение которой
![]()
Из 32 г серы — 22,4 л SO2,
из х г серы — 400 л SO2.
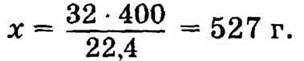
11.23. Оксид серы (IV) при взаимодействии с водой образует сернистую кислоту H2SO3:
![]()
соли которой называются сульфитами. Сернистая кислота — нестойкая, существует только в разбавленных растворах и быстро разлагается на воду и оксид серы (IV). Поэтому при взаимодействии сульфитов с сильными кислотами образуется SО2:
![]()
Чтобы обработать таким способом погреб, надо сульфит натрия в двух-трех кислотоустойчивых неглубоких емкостях, например в пластмассовых кюветах, поместить в верхней части погреба и добавить 10%-ной серной кислоты. Очень важно, чтобы емкости находились в верхней части погреба, так как оксид серы (IV) тяжелее воздуха. Конечно, предварительно надо рассчитать, сколько потребуется сульфита натрия и серной кислоты. Необходимо отметить, что это довольно дорогой способ обработки, дороже, чем сжигание серы, и пользоваться им целесообразно только для обработки небольших объемов и тогда, когда нет возможности получить оксид серы (IV) другим способом.