Химия ЕГЭ - 1000 заданий с ответами и решениями - 2018 год
Реакции ионного обмена - Химическая реакция - ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ
Тесты с выбором ответа с решениями
1. В ионном уравнении реакции записываем в виде ионов
1) Mg(OH)2
2) CuSO4
3) H2S
4) BaSO4
2. В ионном уравнении реакции записываем в виде молекул
1) Н2O
2) FeCl3
3) NaOH
4) Na2CO3
3. Гидроксид цинка реагирует с раствором гидроксида натрия, поскольку в ходе этой реакции образуется
1) сильный электролит
2) газ
3) осадок
4) комплексное соединение
4. Реакция в растворе не идет между
1) КОН и FeCl3
2) ВаСl2 и H2SO4
3) NaCl и CuSO4
4) NaHCO3 и НСl
5. Какие ионы реагируют при сливании растворов К2СO3 и НСl?
![]()
6. Какая пара ионов участвует в химической реакции при сливании растворов хлорида кальция и фосфата натрия?
![]()
7. Для реакции Ва(ОН)2 + H2SO4 = BaSO4 + 2Н2O сумма коэффициентов в сокращенном ионном уравнении равна
1) 7
2) 6
3) 9
4) 8
8. Сумма коэффициентов в сокращенном ионном уравнении взаимодействия 1 моль гидроксида алюминия с 1 моль гидроксида натрия в водном растворе равна
1) 8
2) 6
3) 4
4) 3
9. Уравнению ![]() соответствует взаимодействие
соответствует взаимодействие
1) КОН с HNO2
2) H2SO4 с Fe(OH)3
3) HF с NaOH
4) КОН с HNO3
10. Уравнению ![]() соответствует взаимодействие
соответствует взаимодействие
1) Аl(ОН)3 с НСl
2) Na[Al(OH)4] с недостатком НСl
3) Na[Al(OH)4] с Н2O
4) Na[Al(OH)4] с избытком НСl
Тесты с выбором ответа для самостоятельного решения
11. В ионном уравнении реакции записываем в виде ионов
1) AgCl
2) Н2СO3
3) HNO3
4) NH3H2O
12. В ионном уравнении реакции записываем в виде молекул
1) Н2O
2) NaOH
3) H2SO4
4) Ва(ОН)2
13. Гидроксид алюминия реагирует с раствором соляной кислоты, поскольку в ходе этой реакции образуется
1) осадок
2) слабый электролит
3) газ
4) комплексное соединение
14. Реакция в растворе не идет между
![]()
15. Какие ионы реагируют при сливании растворов (NH4)2SO4 И КОН?
![]()
16. Какая пара ионов участвует в химической реакции при сливании растворов сульфита натрия и азотной кислоты?
![]()
17. Для реакции FeS + 2НСl = FeCl2 + H2S сумма коэффициентов в сокращенном ионном уравнении равна
1) 7
2) 6
3) 5
4) 4
18. Сумма коэффициентов в сокращенном ионном уравнении взаимодействия гидроксида цинка с избытком раствора гидроксида натрия равна
1) 4
2) 5
3) 6
4) 7
19. Уравнению ![]() соответствует взаимодействие
соответствует взаимодействие
![]()
20. Уравнению ![]() соответствует взаимодействие
соответствует взаимодействие
1) Zn(OH)2с NaOH
2) ZnSO4 с недостатком NaOH
3) ZnCl2 с водой
4) Zn(NO3)2 с избытком КОН
Ответы на тесты раздела 1.4.6
1. 2 2. 1 3. 4 4. 3 5. 1 6. 2 7. 3 8. 4 9. 4 10. 2 11. 3 12. 1 13. 2 14. 4 15. 3 16. 4 17. 3 18. 1 19. 3 20. 4
Решения тестов раздела 1.4.6
Решение 1. В ионных уравнениях реакций соединения записываются в том виде, в каком они присутствуют в растворе. Сильные электролиты записываются в виде ионов, а слабые электролиты, малорастворимые вещества и газы — в виде молекул. Например, для уравнения реакции ![]()
![]() в полном ионном уравнении осадок
в полном ионном уравнении осадок ![]() , слабый электролит Н2O и газ
, слабый электролит Н2O и газ ![]() записываются в виде молекул, а сильные электролиты НСl и СаСl2 — в виде ионов. Имеем полное ионное уравнение:
записываются в виде молекул, а сильные электролиты НСl и СаСl2 — в виде ионов. Имеем полное ионное уравнение:
![]()
Сокращая хлорид-ионы, получаем сокращенное ионное уравнение:
![]()
Среди перечисленных в задании соединений в виде молекул записываются в ионных уравнениях: осадки Mg(OH)2и BaSO4, а также слабый электролит H2S. Растворимая соль CuSO4 является сильным электролитом и записывается в виде ионов.
Ответ: 2.
Решение 2. Среди перечисленных в задании соединений в виде молекул в ионных уравнениях записывается слабый электролит Н2О. Растворимые соли FeCb и Na2CO3, а также растворимое основание NaOH являются сильными электролитами и записываются в виде ионов.
Ответ: 1.
Решение 3. Ионные реакции идут в сторону образования осадков, газов, слабых электролитов или комплексных ионов. Гидроксид цинка реагирует с раствором гидроксида натрия, поскольку в ходе этой реакции образуется комплексное соединение тетрагидроксоцинкат натрия Na2[Zn(OH)4]. Это видно из соответствующих уравнений реакции:
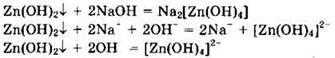
Ответ: 4.
Решение 4. Если в ходе реакции между ионами не образуется осадков, газов, слабых электролитов или комплексных ионов, то эти ионы не взаимодействуют между собой.
Вещества КОН и FeCl3 взаимодействуют, поскольку образуется осадок ![]() Вещества ВаСl2 и H2SO4 взаимодействуют, поскольку образуется осадок
Вещества ВаСl2 и H2SO4 взаимодействуют, поскольку образуется осадок ![]() Вещества NaCl и CuSO4 не взаимодействуют, поскольку образуются растворимые соли Na2SO4 и СuСl2. Вещества NaHCO3 и НСl взаимодействуют, поскольку образуются слабый электролит Н2О и газ СО2.
Вещества NaCl и CuSO4 не взаимодействуют, поскольку образуются растворимые соли Na2SO4 и СuСl2. Вещества NaHCO3 и НСl взаимодействуют, поскольку образуются слабый электролит Н2О и газ СО2.
Ответ: 3.
Решение 5. Реакция между растворами К2СО3 и НСl идет в соответствии с уравнениями:
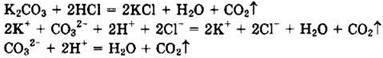
Из сокращенного ионного уравнения видно, что взаимодействуют ионы СO32- и 2Н+.
Ответ: 1.
Решение 6. Реакция между растворами хлорида кальция СаСl2 и фосфата натрия Na3PO4 идет в соответствии с уравнениями:
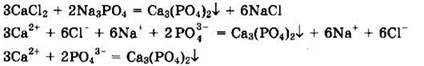
Из сокращенного ионного уравнения видно, что взаимодействуют ионы Са2+ и РO43-.
Ответ: 2.
Решение 7. Напишем уравнения реакции:
![]()
Полное и сокращенное ионные уравнения совпадают друг с другом. Сумма коэффициентов в этом уравнении равна 9.
Ответ: 3.
Решение 8. Запишем молекулярное и ионные уравнения реакции:
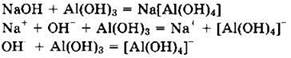
Сумма коэффициентов в сокращенном ионном уравнении равна 3.
Ответ: 4.
Решение 9. Наличие в сокращенном ионном уравнении ионов Н+ и ОН- указывает, что исходные кислота и основание являются сильными электролитами. Соединения КОН и HNO2 не подходят, поскольку HNO2 является слабым электролитом и в ионном уравнении записывается в виде молекулы HNO2, которой нет в сокращенном ионном уравнении. Аналогично не подходят ни соединения H2SO4 и Fe(OH)3, ни соединения HF и NaOH, поскольку Fe(OH)3и HF являются слабыми электролитами и записываются в ионных уравнениях в виде молекул. Соединения КОН и HNO3 являются сильными электролитами. Запишем уравнения реакции между ними и убедимся, что действительно получается требуемое сокращенное ионное уравнение:
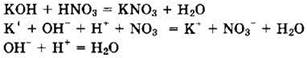
Ответ: 4.
Решение 10. Амфотерным гидроксидам соответствуют два ряда солей. Так, гидроксиду алюминия Аl(ОН)3 соответствуют соли АlСl3 и Na[Al(OH)4].
В ряду соединений ![]() переход от AlCl3 к Аl(ОН)3 и далее к Na[Al(OH)4] идет при постепенном добавлении NaOH, а переход от Na[Al(OH)4] к Аl(ОН)3 и далее к AlCl3 идет при постепенном добавлении НСl. Поэтому для получения Аl(ОН)3 надо к Na[Al(OH)4] прибавить недостаток НСl. Напишем соответствующие уравнения:
переход от AlCl3 к Аl(ОН)3 и далее к Na[Al(OH)4] идет при постепенном добавлении NaOH, а переход от Na[Al(OH)4] к Аl(ОН)3 и далее к AlCl3 идет при постепенном добавлении НСl. Поэтому для получения Аl(ОН)3 надо к Na[Al(OH)4] прибавить недостаток НСl. Напишем соответствующие уравнения:
![]()
![]()
При добавлении к Na[Al(OH)4] избытка HCl реакция идет следующим образом:
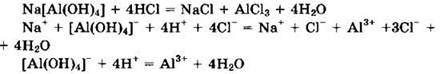
Ответ: 2.